|
琉球大学のトーマ・クラウディア准教授・大倉信彦助教、沖縄科学技術大学院大学(OIST)のブルーノ・ホンベル博士らの研究チームによる成果が、2023年9月15日にスイスの学術雑誌「Frontiers in Cellular and Infection Microbiology」誌のオンライン版で公開されました。 |
<発表のポイント>
-
レプトスピラ症を引き起こす細菌、レプトスピラは、隣り合う細胞同士を「接着する装置」を壊すことによって全身へと広がります。
-
本研究グループは、レプトスピラが細胞のタンパク質分解システムをハイジャックすることによって、細胞同士の接着に必要なp0071とp120-カテニンが分解され、細胞同士が引き剥がれることを発見しました。
-
レプトスピラが細胞同士を引き剥がす仕組みを判明したことから、新規治療薬開発への応用が期待できます。

<内容>
【研究の背景】
レプトスピラ症は熱帯・亜熱帯地域に多く見られる人獣共通感染症の一種で、原因細菌のレプトスピラがネズミなどの保菌動物の尿で汚染された水や土壌からヒトに感染することで発症します。感染症法で届出対象とされていますが、その臨床症状には発熱や筋肉痛など風邪に似た症状の軽症型から黄疸・出血症状・多臓器不全などを伴う重症型まで多様性があるため、確定診断が難しい感染症として知られています。初診が遅れ重症化すると死に至ることもあります。沖縄県での患者発生は他県に比べ多く(届出件数の半数が沖縄)、2022年10月には16年ぶりに死亡例が発生し、2023年9月には竹富町西表島で河川が感染源となった集団発生などが報告されています。レプトスピラ症の治療としては抗菌薬による早期治療が効果的ですが、抗菌薬の投与による副作用などが問題となっており、新たな治療法の開発が求められています。
レプトスピラ症の原因細菌であるレプトスピラは、皮膚・粘膜から血流に入り、肺や腎臓などの標的臓器へと拡がります。体内に侵入したレプトスピラは、コルク栓抜きのような形状で回転運動しながら組織内を移動することがわかってきました(図1)。一方、皮膚や臓器にはもともと細胞間接着装置(接着装置)があり、隣り合う細胞同士を接着させることで、臓器の構造と感染阻止を含む生理機能を維持しています。接着装置は、細胞膜に存在するタンパク質カドヘリン(1)と細胞内裏打ちタンパク質(p0071とp120-カテニン)などから構成されています。病原細菌は様々な戦術を駆使して、これらのタンパク質の機能を撹乱し、感染を成立させます。本研究グループはこれまで、レプトスピラがカドヘリンの細胞内取り込みを誘導することを明らかにしてきましたが、詳しいメカニズムは未解明のままでした。

【研究成果の概要】
レプトスピラがどのように標的臓器に辿り着くかを理解することは、レプトスピラ症の重症化と本菌の全身への広がりを遮断するために重要です。本研究では、レプトスピラの接着装置破壊戦略を明らかにするために、近位尿細管上皮細胞(2)(renal proximal tubular cells, RPTEC)を用いて基底側からレプトスピラで感染させました。次に、感染4時間後と24時間後に感染細胞を回収し、レプトスピラが感染したRPTECでどのタンパク質が減少するかを調べました(図2)。
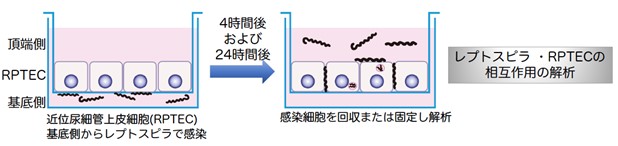
図2. レプトスピラによる接着装置の破壊戦略の解析。近位尿細管上皮細胞(RPTEC)は一層になるように培養し、細胞同士が接着していることを確認し、基底側からレプトスピラで感染させた。
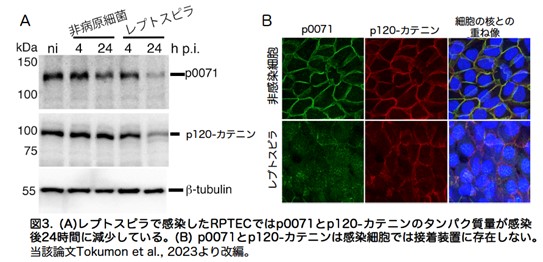
その結果、カドヘリンを細胞膜に局在させるために必要なタンパク質(p0071とp120-カテニン)が感染24時間後には分解されていることが明らかになりました (図3)。
接着装置から遊離したp0071がタンパク質を分解するリソソーム(3)に移行していることが判明したため、レプトスピラはリソソームを利用しp0071とp120-カテニンを分解するという仮説をたてました。しかしながら、リソソーム単独を阻害する実験ではタンパク質の分解は抑制できませんでした。従って、p0071とp120-カテニンは別の、あるいは複数の経路で分解されていると考えられました。そこで、真核細胞に存在するもう一つのタンパク質分解系「ユビキチン・プロテアソーム系、Ubiquitin Proteasome System, UPS」(4)の阻害剤との組み合わせを試みました。実験の結果、リソソームとUPSを同時に阻害することによってp120-カテニンの分解を抑制することに成功し、p120-カテニンが接着装置に止まることがわかりました(図4A)。また、FIB-SEMトモグラフィ法(5)にて阻害剤の組み合わせでRPTEC同士の接着が保たれ、細胞層がが維持されていることが明らかになりました (図4B, 4C)。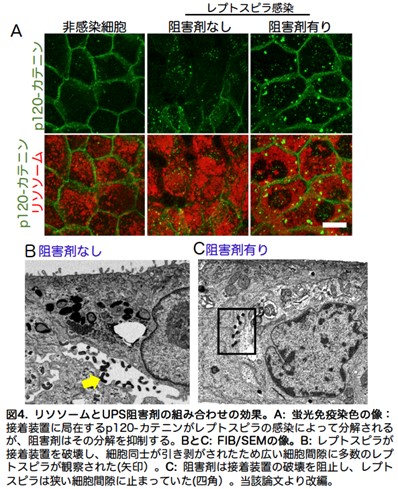
一方、p0071の分解はZ-VAD-FMK阻害剤で抑制され、レプトスピラは複数の”武器”を利用しながら接着装置のタンパク質を分解することがわかりました(図5)。レプトスピラはこの戦術で、効率よく、確実に細胞と細胞を引き剥し感染を成立させると考えられます。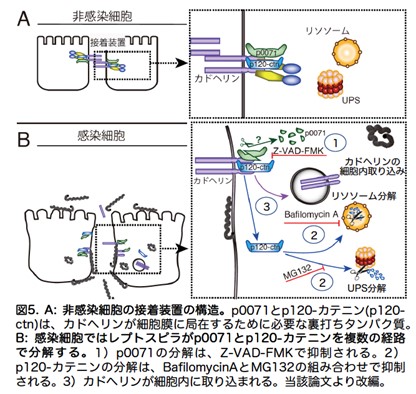
【研究成果の意義】
本研究でレプトスピラは細胞のタンパク質分解システムをいわばハイジャックすることによって接着装置を構成するp0071とp120-カテニンの分解を誘導し、接着装置を破壊することが判明しました。本研究で得られた新規知見は、レプトスピラ症の病態形成メカニズムの理解に寄与し、本感染症を制御するためには複数の経路が抑制可能であることを明らかにしました。
レプトスピラ症の抗菌薬による早期治療は効果的ですが、抗菌薬使用に伴って死んだレプトスピラの菌体成分であるリポ多糖が体内に多量に放出され、これが原因となるエンドトキシン反応(Jarisch-Herxheimer反応)(6)が問題となっています。また、症状が軽症の場合でも菌が腎臓に定着し、慢性的腎不全の原因になり得ることも明らかになってきました。そのため、環境中のレプトスピラに日常的にさらされる職業(農業、家畜の飼育、川のエコツーリズムのガイドなど)では、レプトスピラ症に対する予防投薬が議論となっています。しかし、病原細菌を徹底的に殺そうとする抗菌薬の使用では耐性菌の出現などの問題があり、新たな治療法の開発が求められています。レプトスピラがどのように細胞のタンパク質分解システムを利用するかを明らかにすることによって、感染の成立や維持に必須の細菌因子や細胞内伝達経路を阻止し、レプトスピラ症をピンポイントで制御できる新たな治療法の開発が期待できます。
【用語解説】
(1)カドヘリン:細胞膜を貫通するタンパク質で、細胞外領域が細胞表面に突き出ており、同じカドヘリン分子同士が結合することによって、向かい合う細胞膜を接着させる。
(2)近位尿細管上皮細胞:腎臓の糸球体の近くにある尿細管の細胞。内腔側の細胞膜は微絨毛によって、著しく面積を増しており、大量の再吸収を行う細胞である。
(3)リソソーム:細胞内に存在する、タンパク質の分解を専門とする小器官。多数の分解酵を含んでいる。
(4)ユビキチン・プロテアソーム系、Ubiquitin Proteasome System, UPS:細胞内のタンパク質分解系であり、目的としたタンパク質だけを厳密に識別して分解するシステム。タンパク質はプロテアソームという分解酵素複合体によって分解される。
(5) FIB-SEM トモグラフィ法: 集束イオンビーム(FIB)と走査電子顕微鏡(SEM)を組み合わせ、細胞と細菌の相互作用などを3次元的に可視化する手法。
(6) Jarisch-Herxheimer反応: レプトスピラなどの細菌感染症抗菌薬治療に引き続いて悪寒、発熱、低血圧などが起こる現象である。
【研究体制と支援】
本研究は、琉球大学大学院医学研究科(細菌学講座、分子解剖学講座)、沖縄科学技術大学院大学、化学物質評価研究機構の共同研究として行われました。また、次の研究助成のもとで行われました:文部科学省・科学研究費補助金(21H02732)、公益財団法人武田科学振興財団研究助成、日本医療研究開発機構(BINDS, JP23ama121004)、および琉球大学外国人客員研究員制度。
【論文情報】
- 論文タイトル:
Degradation of p0071 and p120-catenin during adherens junction disassembly by Leptospira interrogans.
(和訳)病原性レプトスピラはp0071とp120-カテニンの分解を誘導し、細胞間接着装置を破壊する - 雑誌名: Frontiers in Cellular and Infection Microbiology
- 著 者: Romina Tokumon1, Isabel Sebastián1, Bruno M. Humbel2, Nobuhiko Okura1, Hidenori Yamanaka3 , Tetsu Yamashiro1 and Claudia Toma1*
* Corresponding author - 1 琉球大学大学院医学研究科、2 沖縄科学技術大学院大学、3 化学物質評価研究機構
- DOI番号:10.3389/fcimb.2023.1228051
- URL:https://www.frontiersin.org/articles/10.3389/fcimb.2023.1228051/full
