| 琉球大学医学部附属動物実験施設 市瀬准教授らの研究チームによる研究成果が、学術雑誌「The Journal of Pathology」誌に掲載されました。 【発表のポイント】 琉球大学医学部市瀬准教授の研究チームは、遺伝子改変マウスを用いた研究によって、皮膚を構成する表皮ケラチノサイトの増殖やがん化の分子メカニズムについての新たな知見を得ました。遺伝子発現を制御するタンパク質であるCBP/p300に、表皮細胞におけるEGFR-Ras-Erkシグナリングを抑制し、表皮細胞の増殖やがん化を抑える働きがあることを新たに見出しました。本研究成果は、沖縄県での有病率が高い、表皮ケラチノサイトの増殖性病変やがんの発生・進展機序の解明に寄与することが期待されます。 |
【発表概要】
私たちヒトを含む生き物は、G,A,T,Cの4文字で書かれた膨大な量の文字列からなる「台本」(ゲノムの塩基配列情報)を持っています。この台本には、生き物固有の形や動きなどを決める壮大なストーリーが描かれていて、それを演じるのは細胞です。ヒトを含む多細胞生物1体を構成する1個1個の細胞は、皆同じ台本を渡されていますが、体の中の役割に応じて、台本の参照箇所やセリフが異なります。台本が正しくても、その内容を正しく表現できないと、台本の描くストーリーが成立しません。そのため、生き物には、役割ごとの台本の正しい使い方や読み方を決めて、失敗がないようにするためのさまざまな仕組みが備わっています。ヒトの命にかかわる疾患である「がん」の場合、台本の文章が書き換えられているために、細胞が本来の役からかけ離れた役を演じてしまうことでストーリーが崩れる(=がんが生じる)例がよく知られています。しかし、台本が正しい場合でも、台本の参照箇所の誤りやセリフの表現の誤りが、がんの発生や進展の原因となることがわかってきています。
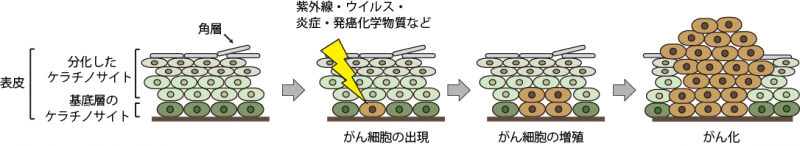
沖縄では皮膚の有棘細胞がん(扁平上皮がん)(注1、図1)や、がん前駆症と考えられる日光角化症(注2)の有病率が、本土と比較して高いことが知られています。地理特性上、日光紫外線の量が多く、日光にあたる時間も長いことが原因のひとつであると考えられていますが、個人個人が持っている遺伝子の「個性」、感染・炎症、代謝、そして加齢など、さまざまな要因の関与も考えられています。琉球大学医学部附属動物実験施設の 市瀬 広武 准教授と市瀬 多恵子 非常勤講師(2018年3月まで東京大学医科学研究所システム疾患モデル研究センターに在籍)の研究チームは、表皮ケラチノサイト(注3)のがん化において、CBPとp300という2種類のよく似た構造および機能をもつタンパク質(以下、CBP/p300と記載、注4)に着目しました。
CBP/p300は、他のタンパク質と一緒になって様々な遺伝子の働きをコントロールする役割を果たすことから、コアクティベーターと呼ばれています。台本のどの箇所を、どのタイミングで、どのような音量や調子のセリフで表現するかを決めていると考えられています。CBP/p300をコードする遺伝子の変異(台本のエラー)は皮膚の有棘細胞がんで高頻度に見つかっていることから、CBP/p300の機能低下が表皮ケラチノサイトの暴走にかかわっている可能性が考えられます。しかし、CBP/p300の機能低下が表皮ケラチノサイトにどのような変化を引き起こすのかはわかっておらず、このCBP/p300が果たす役割について、実験モデルを用いて検証する必要がありました。
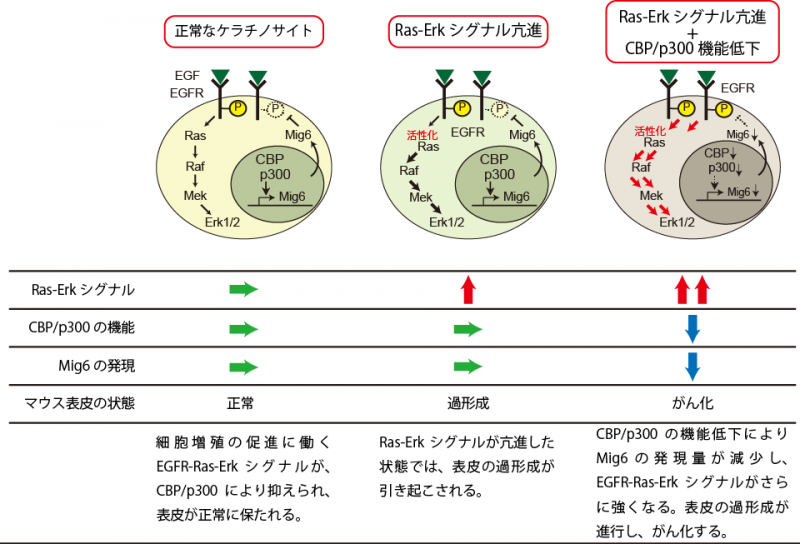
市瀬准教授らの研究チームは、表皮ケラチノサイトの行き過ぎた増殖におけるCBP/p300の役割に焦点を置きました。表皮ケラチノサイトが過剰に増える遺伝子改変マウスを用いて、CBP/p300の機能低下が表皮ケラチノサイトに及ぼす影響を調べた結果、CBP/p300の機能低下が、がん化の促進に働くことが知られるRas-Erkシグナル(注5)を増強し、表皮ケラチノサイトのがん化を促進する方向に働くことを見出しました(図2)。表皮ケラチノサイトでは、細胞増殖因子の一種、EGFファミリーに応答するEGF受容体(EGFR) (注6)が発現していて、表皮の正常な発生と維持に寄与していますが、このEGFRからのシグナルが異常に高まると、上皮のがん化が促進されます。CBP/p300の機能が低下した状態では、このEGFRからRas-Erkに至るシグナルが亢進していました。EGFRシグナルを抑制するタンパク質Mig6の遺伝子発現レベルの減少が、その背景にあることを突き止めました。
この成果は、病理学・腫瘍学分野での評価が高い、英国・アイルランド病理学会の学術誌The Journal of Pathology(2017年のインパクトファクター6.25)に掲載されます。CBP/p300がどのような分子メカニズムを介してMig6の遺伝子発現レベルの維持に寄与しているのか、Mig6のみを介してEGFR-Ras-Erkシグナルの過剰な活性化を抑制しているのか、という点については更に検討していく必要がありますが、表皮ケラチノサイトにおけるCBP/p300の役割を、動物モデルを用いて明らかにした現段階での成果が評価されました。研究は基礎的な段階ですが、沖縄県での有病率が高い皮膚に生じるがんや増殖性病変の研究において、表皮ケラチノサイトからのがんの発生、および進行の機序の解明など、CBP/p300に関する本研究の知見が役に立つかも知れません。今後の研究の進展に、ご期待下さい。
(注1)表皮ケラチノサイトから発生する皮膚がん。
(注2)日光の紫外線が原因となって生じる、表皮ケラチノサイトの異常。
(注3)表皮とは、皮膚の表面にある細胞の層である(図1、左)。その大部分を構成する細胞が、表皮ケラチノサイト(角化細胞)である。表皮の層構造は、ケラチノサイトとそれが変化(分化)した細胞で構成されている。表皮の最も内側に、増殖する能力をもつケラチノサイトで構成される基底層がある。基底層のケラチノサイトは増殖する一方、形や機能が異なるタイプのケラチノサイトに変化しながら、より外側(体表に近い側)の層構造を形作る。最も外側には、核のない死んだケラチノサイトが重なった丈夫な層(角層)が作られるが、少しずつ自然にはがれ落ち、内側で新しく作られて表面に向かって押し上げられていく角層に置き換わっていく。
(注4)CBP/p300は、遺伝子発現制御に寄与する、タンパク質のアセチル化酵素である。構造や機能がきわめてよく似ているため、CBP/p300という1つのファミリーとして考えられている。一部のがんでCBP/p300の遺伝子変異が見つかることから、その機能の異常ががん化に関係していることはわかっているが、メカニズムがよくわかっていない。
(注5)タンパク質同士の相互作用を介した、さまざまな情報伝達の方法が細胞の中に存在するが、Ras-Erkシグナルはその中のひとつである。多くのがんで、Ras-Erkシグナルの過剰な活性化を引き起こす原因となる遺伝子変異が見つかっている。
(注6)細胞外からのシグナル(EGFファミリーとよばれるタンパク質)を、細胞の中に伝えるための、いわば受付・連絡係。遺伝子変異によるEGFRシグナルの亢進が、上皮がんの発生や進展に関与する。
【論文情報】
(1) 論文タイトル
CBP/p300 antagonises EGFR-Ras-Erk signalling and suppresses increased Ras-Erk signalling-induced tumour formation in mice
マウスにおいて、CBP/p300はEGFR-Ras-Erkシグナリングを弱め、Ras-Erkシグナリング亢進による腫瘍形成を抑える
(2) 雑誌名 The Journal of Pathology
(3) 著者 Taeko Ichise, Nobuaki Yoshida, Hirotake Ichise*
(4) DOI番号 10.1002/path.5279
(5) アブストラクトURL
https://www.ncbi.nlm.nih.gov/pubmed/30953353
https://onlinelibrary.wiley.com/doi/abs/10.1002/path.5279