|
<発表のポイント> ◆光合成によって増殖する単細胞藻類シゾンを用いて、組換えタンパク質を高効率・高純度で得るタンパク質生産システム“CZON-PURE(シゾン・ピュア)”を確立しました。 ◆新たに発見した非常に強い遺伝子発現活性を示すHiXプロモーターを利用することにより、藻類を利用した組換えタンパク質生産システムとしては極めて高い生産性を実現しました。 ◆安価な無機塩の培地と、光、二酸化炭素によって培養が可能なほか、ウイルスやバクテリアの混入リスクも非常に低いため、低コストかつ安全性の高い、医療研究や産業利用などを目的とした組換えタンパク質の大規模生産に貢献することが期待されます。 |
<概要>
東京大学大学院理学系研究科の茂木祐子特任助教、吉田大和准教授、琉球大学研究基盤統括センターの八木沢芙美准教授らによる研究グループは、単細胞紅藻シゾン(注1)を用いて、組換えタンパク質を高効率・高純度で得るタンパク質生産システム“シゾン・ピュア”を確立しました。
本研究では、シゾンで細胞周期を通じて特に高い遺伝子発現を示すHiXプロモーターを同定し、これを利用した発現ベクター(注2)を開発することで、組換えタンパク質(注3)を安定して高レベルに発現・蓄積できることを示しました。さらに、シゾンが細胞壁を持たないという特性を活かし、細胞を凍結して溶かすだけの簡単な操作でタンパク質を抽出し、一般的なアフィニティ精製(注4)や免疫沈降法(注5)により高純度に精製できることを実証しました。従来は藻類や植物などの光合成生物から十分な量の組換えタンパク質を精製することは非常に困難でしたが、本成果により高価な抗生物質や有機物を使用せず、またウイルスやバクテリアの混入リスクが極めて少ないクリーンで安全な組換えタンパク質生産の選択肢が広がることが期待されます。
<発表内容>
研究の背景
タンパク質は細胞の働きを担う基本要素であり、その機能や仕組みを調べるには目的タンパク質を十分な量と品質で得ることが欠かせません。また抗体や酵素などのタンパク質は、研究に加えて医療・産業分野でも幅広く利用されています。こうした需要に応えるため、さまざまな生産・精製法が発達してきましたが、培養にかかるコストや生産規模拡大の課題に加え、ウイルスや細菌などの混入を防ぐための品質管理負担が課題となっています。
近年、微細藻類は光合成によって空気中の二酸化炭素と光エネルギーを利用して増殖することから、環境負荷の小さい生産基盤として注目されています。しかし多くの藻類では、組換えタンパク質を安定して高発現させることや、回収・精製を効率よく行うこと、遺伝子操作の柔軟性などに課題が残っています。そこで本研究では、細胞壁を持たず、高温・強酸性条件でも増殖できる単細胞紅藻シゾンに着目し、タンパク質生産・精製の新しい基盤技術の確立を目指しました。
研究内容と成果
単細胞紅藻シゾンを用いた高収率な組換えタンパク質生産システム“シゾン・ピュア”を確立するため、まず組換えタンパク質を安定して高レベルに発現させるための遺伝子発現制御配列の探索を行いました。シゾンのトランスクリプトームおよびトランスラトーム解析(注6)によって得られたデータを比較した結果、細胞周期を通じて最も強い発現活性を示す遺伝子を見出し、強力な恒常発現プロモーター(注7)であるHiXプロモーターを同定しました(図1)。
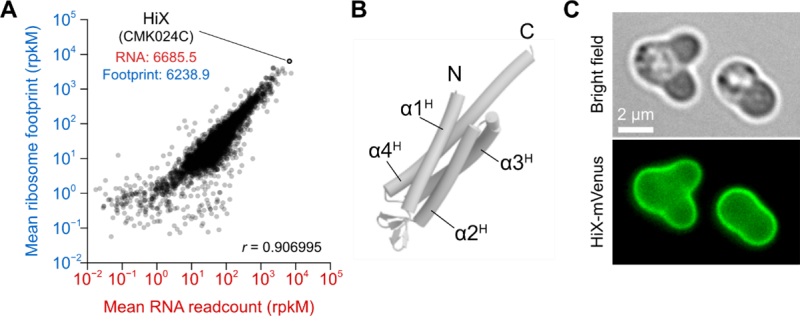
図1:シゾンにおいて最も高い発現レベルを示す機能不明遺伝子HiX
(A)トランスクリプトーム・トランスラトーム解析により、シゾンにおいてRNA転写レベルとタンパク質翻訳レベルが最も高い機能不明遺伝子を同定し、HiXと命名した。
(B)HiXタンパク質の三次元構造シミュレーション。4つのヘリックスが束構造を取ることが予想された。
(C)蛍光タンパク質mVenusを融合したHiX-mVenusの細胞内局在。細胞膜への集積が確認された。
次に、HiXプロモーターを組み込んだ発現ベクターpHiXを設計し、シゾン細胞内で目的タンパク質を高発現させる遺伝子導入系を構築しました。モデルタンパク質として蛍光タンパク質mVenusを導入したところ、形質転換したシゾン細胞の細胞質に強い蛍光シグナルが観察され、分裂期・非分裂期のいずれでも発現が安定して維持されることを確認しました(図2)。
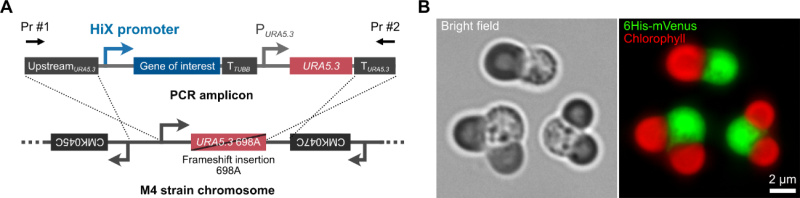
図2: HiXプロモーターによって制御されるmVenus遺伝子カセットを組み込んだシゾン
(A)HiXプロモーターによって発現制御されるmVenus遺伝子カセットをシゾン染色体DNAへ相同組み換えによって導入。
(B)高い発現レベルを示す蛍光タンパク質mVenusの細胞内局在。
シゾンは藻類であるにもかかわらず強固な細胞壁を持たないため、細胞を凍結して溶かすだけの簡単な操作で細胞内容物を効率よく抽出できることを実証しました(図3)。得られた抽出液から、一般的な金属アフィニティ精製(IMAC)を用いて目的タンパク質を高純度に精製でき、総可溶性タンパク質あたり13.9 mgという極めて高い回収量で精製できることを示しました(図4)。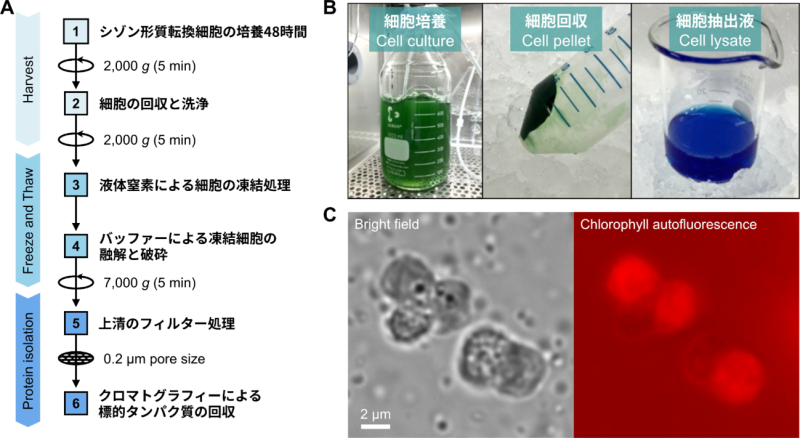
図3:シゾンから組換えタンパク質を精製するフロー
(A)シゾンから組換えタンパク質を精製するプロセス。
(B)精製過程の様子。細胞の培養(左)後、遠心分離によって細胞を回収(中)、そして1回の凍結・融解処理によって細胞抽出液を得る(右)。
(C)凍結融解後は、細胞膜が破壊されることにより、膜タンパク質を除くほぼ全ての可溶性タンパク質が溶液中へと流出する。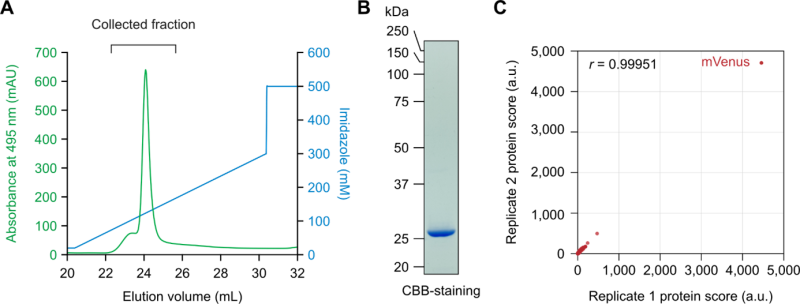
図4:液相クロマトグラフィーによるシゾン細胞破砕液から標的タンパク質の精製
(A)Ni-NTAアフィニティーカラムを用いたヒスチジンタグ融合mVenusタンパク質の精製。
(B)精製したHis-mVenusのSDS-PAGE電気泳動象。
(C)精製されたmVenusタンパク質画分の質量分析。横軸と縦軸は異なる精製実験サンプルによる技術的反復を示す。
さらに、蛍光タンパク質mVenusだけでなく、近年その有用性が高く認識されている単鎖抗体(ナノボディ)(注8)についても、シゾンで発現・精製に成功しました。 シゾンの培養には特殊な培養装置は必要なく、大腸菌などを培養する恒温培養器に市販のLEDライトの光源があれば可能です。また培養した細胞は凍結保存でき、培養スケールの拡大も容易であることから、運用面でも扱いやすいワークフローになっています。さらに細胞培養には有機物や抗生物質といった高価な試薬を必要とせず、安価な無機塩と光、二酸化炭素があれば培養可能です。また培地が酸性であるため、バクテリアなどの混入リスクが極めて低く、組換えにはウイルスを用いないため、経済性および安全性についても非常に有用な性質を備えています。以上の結果から、シゾン・ピュアは「高い発現効率」、「簡便な抽出方法」、「高純度な組換えタンパク質精製」を一体化した、シゾンを用いるタンパク質生産・精製プラットフォームとして有効であることが実証されました。
<今後の展望>
十分な量と高い品質を備えた組換えタンパク質を得ることは、機能解析や相互作用解析、構造解析など幅広い分子生物学・医科学研究の出発点となります。さらに今後、対象タンパク質の多様化や発現・培養条件の最適化を進めることで、基礎生物学に加えて医療・産業分野における組換えタンパク質を利用した研究開発にも貢献することが期待されます。
〇関連情報:
「ゲノム編集と4種オルガネラの蛍光可視化を同時に実現」(2021/11/11)
https://warp.ndl.go.jp/web/20230513005318/www.s.u-tokyo.ac.jp/ja/press/2021/7606/
「ミトコンドリアへ運ぶタンパク質を見極める」(2024/7/24)
https://www.s.u-tokyo.ac.jp/ja/press/10424/
「細胞増殖時に創られる全てのタンパク質を同定」(2025/1/10)
https://www.s.u-tokyo.ac.jp/ja/press/10620/
発表者・研究者等情報
東京大学
大学院理学系研究科 生物科学専攻・生物学科
吉田 大和 准教授
茂木 祐子 特任助教
津島 彰悟 修士課程
永井 祥太郎 学部生
琉球大学
研究基盤統括センター
八木沢 芙美 准教授
総合技術部
儀間 真一 マネージャー
論文情報
雑誌名:Journal of Cell Science
題 名:A high-yield protein expression platform in the unicellular red alga Cyanidioschyzon merolae
著者名:Yuko Mogi, Shogo Tsushima, Shotaro Nagai, Shinichi Gima, Fumi Yagisawa and Yamato Yoshida*(*責任著者)
DOI:10.1242/jcs.264207
URL:https://doi.org/10.1242/jcs.264207
研究助成
本研究は、JST創発事業「オルガネラ分裂制御による細胞自律性の創発」(課題番号:JPMJFR2316,研究代表者:吉田大和)、科学研究費助成事業「リアルタイム蛍光観察を基盤としたオルガネラ分裂リングの収縮機構の解析」(課題番号: 22H02653,研究代表者:吉田大和)、「紅藻におけるMYB転写因子とポリリン酸代謝が介するリン酸飢餓応答機構の解明」(課題番号: 25K09727,研究代表者:八木沢芙美)の一環として行われました。また本論文は東京大学によるオープンアクセス論文出版支援により無償公開予定です。
用語解説
(注1)シゾン
温泉のような酸性の高温環境に生息する単細胞紅藻Cyanidioschyzon merolaeの略称です。シゾンは単純な細胞構造に加えてゲノム構造もシンプルであり、細胞核ゲノムにコードされている遺伝子は僅かに4778遺伝子しかありません。現在では“シゾン・カッター法”などのゲノム編集をはじめとするさまざまな遺伝子改変技術も確立しており、真核生物の基本原理を解析するモデル生物となっています。
(注2)発現ベクター
発現ベクターとは、目的の遺伝子を細胞に導入し、タンパク質を作らせるための人工DNA分子です。プロモーターなどの制御配列を組み込むことで、目的タンパク質を効率よく生産できます。
(注3)組換えタンパク質
組換えタンパク質とは、人工的に導入した遺伝子から作られるタンパク質です。医薬品や研究用試薬などの生産にも広く利用されています。本研究では、シゾン細胞内で目的の組換えタンパク質を高レベルに安定発現させることに成功しました。
(注4)アフィニティ精製
アフィニティ精製とは、特定のタンパク質だけを選び出して取り出す方法です。目的タンパク質に特定のタグを付け、そのタグに結合するビーズを用いて回収することで、高純度に精製する方法です。
(注5)免疫沈降法
免疫沈降法は、目的タンパク質に特異的に結合する抗体を利用して、そのタンパク質を細胞抽出液から選択的に回収する方法です。抗体をビーズに固定し、結合したタンパク質を沈殿として分離します。
(注6)トランスクリプトームおよびトランスラトーム解析
トランスラトーム解析は、生物の全ゲノムにわたる遺伝子発現を翻訳(タンパク質合成)の観点から網羅的に解析する手法です。この解析では、細胞や組織内のリボソームに結合しているmRNAを特定し、その配列を解析することで、どの遺伝子がどの程度タンパク質として実際に合成されているかを明らかにします。リボソームプロファイリング技術により、mRNAがどの程度翻訳されているか、さらには翻訳開始点や翻訳停止点など、翻訳が起こる位置まで詳細に調べることができます。また、この手法により、遺伝子の翻訳効率(mRNAがどの程度タンパク質に変換されているか)の解析も可能です。従来のトランスクリプトーム解析(RNA-Seq)はmRNAの総量を測定するものの、それが実際に翻訳されているかはわかりません。一方、トランスラトーム解析は翻訳されているmRNAに焦点を当てるため、タンパク質合成に直結した詳細な情報を提供します。
(注7)恒常発現プロモーター
恒常発現プロモーターとは、細胞周期や環境変化に左右されず、遺伝子を安定して発現させるDNA配列です。本研究では、シゾンにおいて特に強力な恒常発現プロモーターであるHiXプロモーターを同定し、組換えタンパク質を高効率で生産できることを示しました。
(注8)ナノボディ
ナノボディは、ラクダ科動物がもつ特殊な抗体の一部から作られた小型抗体です。通常の抗体よりも小型で安定しており、医療や研究分野で注目されています。本研究では、シゾンを用いてナノボディを高効率に生産できることを示しました。